Beschriftungslaser
Beschriftungslaser
Laserbearbeitung
Laserbeschriftung nach UDI
-
Tags:
- Medizintechnik , Laserbeschriftung , Laserglühen
UDI ist eine Abkürzung für Unique Device Identification. Die Identifizierung von Medizinprodukten trägt zur Verbesserung der Sicherheit im medizinischen Bereich bei.
Im Dezember 2013 veröffentlichte das International Medical Device Regulators Forum (IMDRF) das UDI-Leitliniendokument, um die globale Kohärenz bei der Einführung des UDI-Systems sicherzustellen.
Derzeit unterliegen nur die USA den UDI-Regeln, aber auch andere Länder übernehmen schrittweise das UDI-System.
Was ist MDR?
Die Verordnung 2017/745 (MDR) über medizinische Geräte, welche die Richtlinie 93/42/EWG (MDD) über medizinische Geräte sowie die Richtlinie 90/385/EWG (AIMDD) über aktive implantierbare medizinische Geräte als Verordnung für im EU-Raum vertriebene medizinische Geräte ersetzt, wurde am 5. Mai 2017 veröffentlicht und trat am 25. Mai 2017 in Kraft. Die MDR-Verordnung wird ab dem 26. Mai 2021 angewendet.
Ab sofort ist die MDR – anstelle der MDD – eine wesentliche Voraussetzung für die CE-Kennzeichnung (das Zeichen, das die Konformität mit den Normen der jeweiligen Bereiche für die angegebenen, im EU-Raum vertriebenen Produkte bestätigt). Die MDR inkludiert die UDI (Unique Device Identification) Kennzeichnung, die Beschriftung von jedem einzelnen Medizinprodukt.
Skalenbeschriftung auf medizinischen Bohrern

Beschriftung von 2D-Codes auf medizinischen Schrauben

Laden Sie den Katalog herunter und erhalten Sie zusätzliche Informationen zu unseren Produkten.
Broschüre herunterladen
UDI-Vorschriften in den USA
Das im September 2013 in den USA in Kraft getretene UDI System wurde ein Jahr später im September 2014 schrittweise verbindlich. Die Einführung des UDI Systems begann zu den folgenden Zeitpunkten in anderen Ländern, in denen die Produktion von Medizinprodukten in den USA besteht.
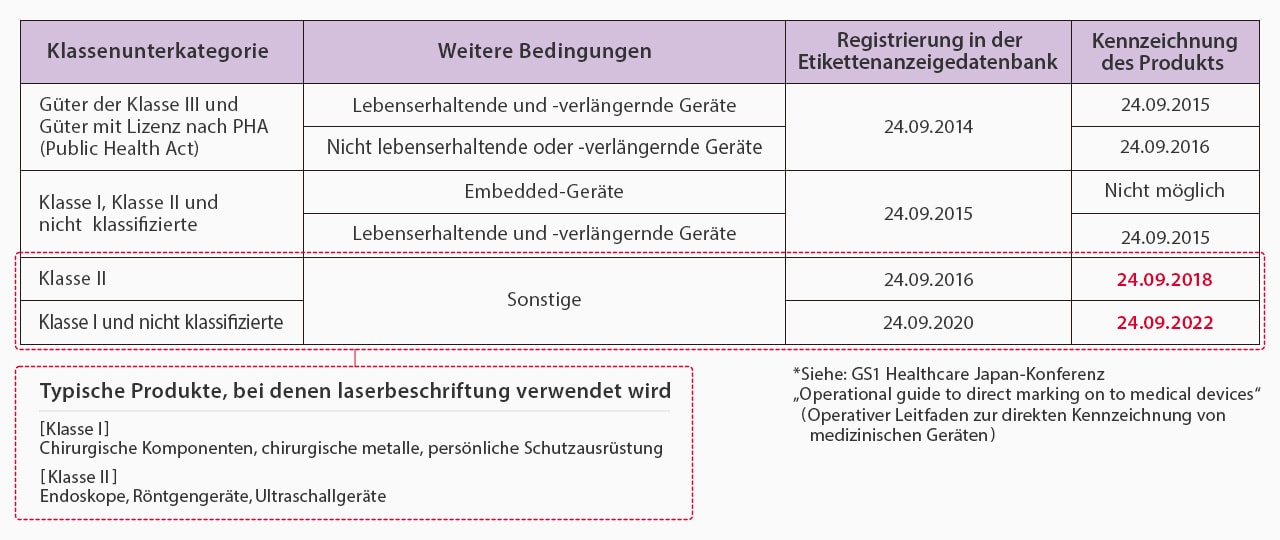
Typische Produkte, bei denen Laserbeschriftung verwendet wird
[Klasse I]
Komponenten im Zusammenhang mit folgenden Geräten, kleine Stahlgegenstände
[Klasse II]
Endoskope, Röntgengeräte, Ultraschallgeräte
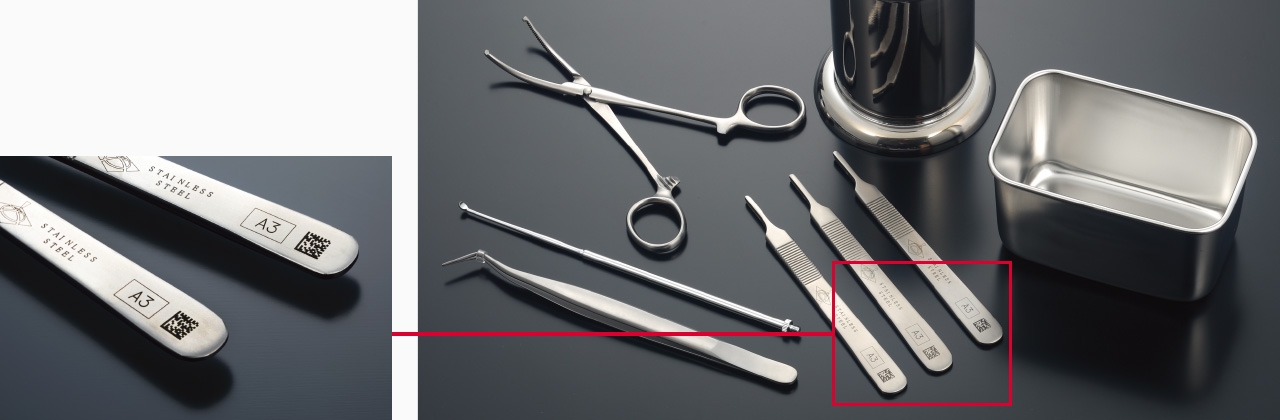
Notwendigkeit der direkten Beschriftung
Medizinische Instrumente wie Stahlinstrumente und Endoskope sind im Allgemeinen kompakt und präzise. Wiederholte Verwendung nach dem Waschen und Sterilisieren ist üblich, daher sind Etiketten wie Papier oder Folie für die UDI Konformität aufgrund des begrenzten Platzes zum Anbringen und der Langzeitbeständigkeit problematisch.
Es gibt auch Risiken, wie z. B. das Ablösen des Etiketts während der Operation und das Zurückbleiben von Fremdpartikeln im Körper eines Patienten.
Diese Bedenken führen zu einem wachsenden Bedarf an Direktbeschriftung.
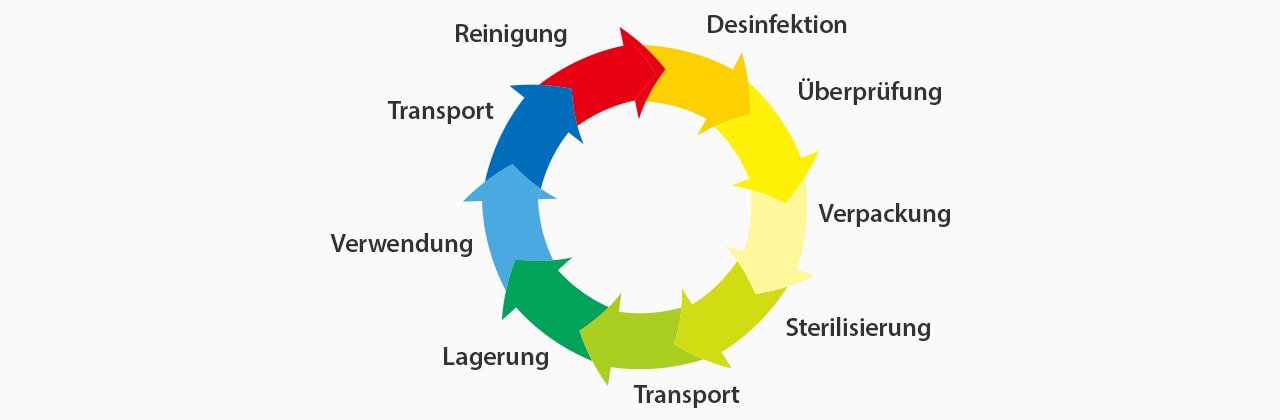
Vorteile der direkten Beschriftung
Die Verwaltung medizinischer Geräte mit direkter Beschriftung für die UDI Verwaltung bietet folgende Vorteile:
- Aufrechterhaltung der Qualität durch die Möglichkeit, zu überwachen, wie häufig Geräte verwendet werden
- Optimierung von Ersatz- und Bestellzeiten
- Verbesserung der Effizienz und Standardisierung von Gerätesätzen
- Nachverfolgung der Instrumente während der einzelnen Prozesse (Standortmanagement)
- Vermeidung von Überschussbestand
- Analyse von Verlust, Diebstahl, Bruch usw.
Welche Art von Beschriftung ist erforderlich?
Die folgenden GS1-Codes werden bei der direkten Beschriftung von medizinischen Geräten für die UDI Konformität verwendet:
- GS1-128
- GS1-Datenmatrix (wenn nicht genügend Platz für einen GS1-128 zur Verfügung steht)
Dem GS1-Code müssen die folgenden UDI konformen Etiketten-Produktinformationen zugewiesen werden:
- 01: GTIN (Produktcode)/10: Chargennummer/17: Ablaufdatum
- 21: Seriennummer/11: Herstellungsdatum
Die zweistellige Nummer wird als AI (Anwendungs-ID) bezeichnet und auf der Anzeige in Klammern dargestellt, sodass sie mit bloßem Auge gelesen werden kann.
2D-Code Laserbeschriftung
Der Kontrastunterschied zwischen schwarzen und weißen Zellen spielt bei der Beurteilung von 2D-Codes eine große Rolle. Ein Beschriftungslaser erzeugt unterschiedliche monochrome Farben, indem die Beschriftungsbedingungen zwischen weißer Beschriftung und Anlassbeschriftung verändert werden

Prinzip der Anlassbeschriftung
Beim Auftreffen des Laserstrahls auf dem zu markierenden Objekt wird der Fokus verschoben, so dass nur Wärme eingeleitet wird. Durch die Wärmeeinwirkung bildet sich an der Oberfläche eine Oxidschicht. Diese Schicht weist eine schwarze Verfärbung auf und wird als Anlassbeschriftung bezeichnet.
Prinzip der weißen Beschriftung
Der Laserstrahl trifft im Fokuspunkt auf das zu markierende Objekt. Ein Teil der Metalloberfläche wird dabei abgetragen, und es wird eine unebene Oberfläche freigelegt. An dieser unebenen Fläche wird das Licht unregelmäßig reflektiert, wodurch der weiße Farbeindruck der Beschriftung entsteht.
UDI jetzt beantragen
Egal für welche Beschriftungsmethode Sie sich am Ende entscheiden: Es ist wichtig, dass Sie Ihre Produkte durch die Zuteilungsstelle mit einer UDI versehen lassen, um sie in der Eudamed Datenbank einzuspeisen. Die Verordnung zur UDI sowie den Durchführungsbeschluss finden Sie auf den Webseiten der Europäischen Union.
Empfohlene Artikel

2D-Codes werden verwendet, um Datumscodes, Chargencodes, Seriennummern und mehr zu speichern. Benutzer, die eine 2D-Code-Beschriftung in Betracht ziehen, sollten diesen Leitfaden zur Laserbeschriftung lesen.



